Aviso de seguridad: actualización de contraindicaciones y advertencias de determinadas máscaras faciales y nasales PHILIPS RESPIRONICS
Es para ciertos modelos de máscaras faciales y nasales de la empresa fabricante PHILIPS RESPIRONICS que contienen imanes que pueden afectar a implantes y productos médicos.
Se informa que la empresa fabricante PHILIPS RESPIRONICS Inc. emitió, de forma voluntaria, un aviso de seguridad de campo indicando que ciertos modelos de máscaras faciales y nasales contienen imanes que pueden afectar el funcionamiento y/o inducir el movimiento / la dislocación de pacientes con implantes u otros tipos de productos médicos que pueden resultar impactados por los campos magnéticos. Este aviso también incluye a miembros del hogar, cuidadores y compañeros de cama que pudieran encontrarse muy próximos a los pacientes que utilicen las máscaras.
El aviso refiere a los siguientes modelos de máscaras faciales y nasales:
- Máscara facial completa de contacto mínimo Amara View
- Máscara facial completa DreamWear
- Máscara nasal con almohadilla sobre la nariz DreamWisp
- Máscaras nasales Wisp y Wisp Youth
- Máscaras para terapia 3100 NC/SP
A continuación, se ilustran las máscaras afectadas y se indican mediante un círculo la disposición de los ganchos craneales magnéticos de las máscaras:

Según la información brindada por el fabricante, RESPIRONICS INC. está actualizando sus notas de contraindicación y advertencia conforme se indica a continuación:
Contraindicación:
El uso de la máscara está contraindicado para los pacientes --y los miembros de su hogar, cuidadores y compañeros de cama que pudieran encontrarse muy próximos a los pacientes que utilicen las máscaras-- con productos implantados que pudieran verse afectados por imanes, entre los que se incluyen, pero no están limitados a:
- Marcapasos
- Desfibriladores Cardioversores Implantables (ICD, por su sigla en inglés)
- Neuroestimuladores
- Válvulas / electrodos / implantes metálicos magnéticos colocados en los miembros superiores, el torso o en una parte superior del cuerpo (por ejemplo: cuello y cabeza)
- Derivaciones de líquido cefalorraquídeo (LCR) (por ejemplo: derivaciones ventriculoperitoneales)
- Clips de aneurisma
- Espirales de embolia
- Dispositivos interruptores de flujo endovascular de aneurismas intracraneales
- Placas, tornillos, cubiertas de orificios de trepanación y dispositivos de reemplazo óseo de materiales metálicos
- Esquirlas metálicas en los ojos
- Implantes oculares (por ejemplo: implantes para glaucoma, implantes retinales)
- Ciertos lentes de contacto con metal
- Implantes para restablecer o equilibrar la audición que contengan un imán implantado (como implantes cocleares, dispositivos de audición de conducción ósea implantados e implantes auditivos de tronco cerebral)
- Componentes de fijación de dentaduras postizas de material magnético
- Clips gastrointestinales metálicos
- Endoprótesis vasculares (stents) metálicas (por ejemplo: para aneurismas, coronarias, traqueobronquiales, biliares)
- Puertos y bombas implantables (por ejemplo: bombas de insulina)
- Estimuladores del nervio hipogloso
- Dispositivos rotulados como no seguros para RM (resonancia magnética)
- Implantes metálicos magnéticos no rotulados para RM o no evaluados a los fines de la seguridad en un campo Magnético
Advertencia:
En la máscara se utilizan imanes con un campo magnético 400 mT de fuerza. A excepción de los dispositivos identificados en la contraindicación, asegúrese de mantener la máscara a una distancia de al menos unos 15,24 cm de cualquier otro implante médico o producto médico que pudiera resultar impactado por los campos magnéticos a fin de evitar posibles efectos de los campos magnéticos localizados.
A raíz de lo acontecido, el Departamento de Tecnovigilancia de la ANMAT se comunicó y reunió con las empresas titulares de registro de los productos médicos involucrados para solicitar información adicional y mantener un canal de comunicación permanente con las empresas importadoras y la subsidiaria de PHILIPS en el país, PHILIPS ARGENTINA S.A.. Asimismo se solicitó ampliar información sobre las medidas adoptadas para realizar un óptimo seguimiento de la acción correctiva de seguridad en campo planteada, monitorear la situación y su impacto en los pacientes, para luego tomar las medidas correspondientes.
Las empresas mencionadas son:
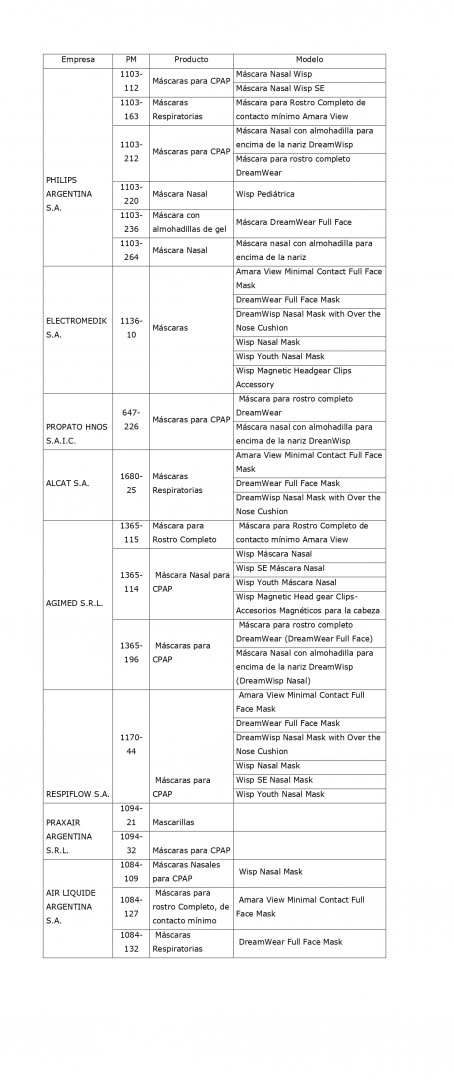
Asimismo, PHILIPS RESPIRONICS comunicó que a la fecha no se han registrado reporte de eventos adversos en América Latina.
Para más información del fabricante ingresar en este enlace
Esta Administración se encuentra monitoreando la situación y procederá a actualizar la información en caso de ser necesario.